Sylentis ha presentado los resultados principales del estudio en Fase I de tolerancia y seguridad con su producto SYL040012 demostrando que la molécula se presenta como un medicamento seguro en las condiciones del ensayo llevado a cabo.
Es la primera vez que se ensaya en España un tratamiento basado en el RNA de interferencia en humanos.
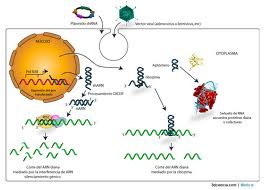
A diferencia de los fármacos tradicionales, el producto que se está investigando va dirigido contra el RNA mensajero, “el paso previo a la formación de las proteínas”.
Los medicamentos y fármacos del mercado se basan en tratamientos contra las proteínas, mientras que este fármaco va contra el componente que da lugar a las proteínas, un paso antes, lo que tiene una serie de ventajas frente a los fármacos habituales (El tiempo de acción de estos productos es mucho mayor que el de un fármaco convencional y los efectos secundarios son menores de manera que se pueden reducir las dosis y evitar efectos colaterales de toxicidad.
El ensayo de Fase I con SYL040012 se realizó en la Clínica Universitaria de Navarra, y reclutó 30 voluntarios sanos, que se dividieron en dos fases de tratamiento; uno fase inicial de tratamiento agudo (una única dosis) y una fase posterior de tratamiento continuado durante 7 días donde se evaluarán dos dosis de SYL040012.
Los ensayos clínicos de Fase I están principalmente diseñados para estudiar la seguridad de un fármaco. Los resultados obtenidos en el estudio Fase I han permitido a Sylentis continuar con estudios en Fases IB y Fase II con los que se espera poder proseguir con el desarrollo clínico de este producto.